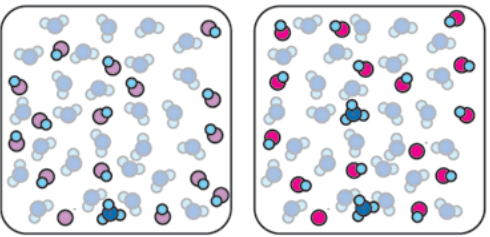
A pergunta enviada enviada foi sobre pH. Para compreender um pouquinho sobre pH nós temos que entender como as
substâncias interagem entre si em solução aquosa. Nós temos aqui representado uma molécula de água e HCl. A molécula de de água (H2O) possui uma
estrutura angular e também é uma molécula polar, afinal de contas o átomo de oxigênio é mais eletronegativo do que o átomo de hidrogênio. Deste modo têm-se uma carga parcial negativa sobre o átomo de oxigênio e uma carga parcial positiva sobre o átomo de hidrogênio. A mesma coisa acontece com a molécula de HCl afinal de contas o átomo de cloro é mais a eletronegativo do que o átomo de hidrogênio.
Quando moléculas polares interagem entre si pode haver rompimento de uma ligação covalente e transferência de hidrogênio para outra a molécula. Nesse caso, forma-se uma molécula de íon hidroxônio e um íon cloreto Cl– que ficará em solução. O mesmo que acontece entre uma molécula de água e uma molécula de HCl vai acontecer entre duas moléculas de água ou seja: duas estruturas polares que são capazes de interagir entre si resultando na transferência de um hidrogênio para outra molécula e rompimento de uma ligação química íons hidroxônio novamente e um íon hidróxido H3O+. Todas essas espécies estão todas dentro de um mesmo compartimento. Dependendo da quantidade de íons H+) esta solução estará ácida (concentração de íons H+ maior do que a concentração de íons OH–). Se houver uma concentração de íons OH– maior do que a concentração de íons H+) a solução estará alcalina.
Há uma medida para quantificar o quanto ácido ou o quanto alcalino está uma soluação: o pH (potencial hidrogeniônico)
* * *
Vejamos esses dois casos: o tetracloreto de carbono (CCl4) e o metano (CH4). Há diferença de eletronegatividade entre o átomo de cloro e o átomo de carbono assim como há diferença de eletronegatividade entre o átomo de hidrogênio e o átomo de carbono. Embora essas ligações químicas sejam polares essas moléculas, como um todo, são apolares isso porque elas são caracterizadas por uma estrutura tetraédrica. Então, se elas são apolares elas não
seriam capazes de interagir com uma molécula de água. Assim, não estaria definido um pH, uma vez que pH não é uma propriedade da estrutura, mas de uma solução resultante das interações intermoleculares – ou seja, se vai produzir em solução íons H+ ou íons OH–.
Se borbulhásses gás metano (CH4) em água e aferíssemos o pH com uma fita indicadora, por exemplo, não haveria mudança no pH da solução.
Dúvidas sobre as teorias ácido-base?
Visite: http://www.quiprocura.net/acido.html.
Dúvidas sobre palaridade e geometria molecular?
Visite: http://quimicasemsegredos.com/polaridade-das-moleculas.php